
时间:2021-02-01 09:49:40来源:美通社
全球性生物制药公司甘李药业股份有限公司(以下简称“甘李药业”)(沪市代码:603087)今天宣布,美国食品药品管理局(FDA)已授予GLR2007快速通道审评资格认定,用于治疗胶质母细胞瘤患者。GLR2007是甘李药业正在开发的一种细胞周期蛋白依赖性激酶4/6(CDK 4/6)抑制剂,用于治疗包括胶质母细胞瘤在内的晚期实体瘤,这种肿瘤是一种侵袭性形式的脑癌,存活率很低。尽管胶质母细胞瘤被认为是一种罕见疾病,但它是最常见的脑和中枢神经系统(CNS)恶性肿瘤,占恶性原发性脑和中枢神经系统肿瘤的45.2%[1]。
胶质母细胞瘤的一年生存率为39.3%。到诊断后第二年和第五年,生存率分别下降到16.9%和5.5%。未经治疗的患者的平均生存时间仅为三个月[2]。当前可用的治疗仅能改善几个月的预后。甘李药业全球临床科学总监黄盈慧表示:“胶质母细胞瘤患者预后差、生存率低,表明这种疾病还需要新的治疗方案以满足治疗需求。” FDA快速通道审评资格认定旨在促进药物开发,加速审评治疗严重疾病和填补医疗亟需的药物。获得快速通道审评资格加强了与FDA的频繁会议和书面沟通。TGLR2007申请还可获得滚动式审评的资格,并且可以进行加速批准和优先审核[3]。
声明:文章仅代表原作者观点,不代表本站立场;如有侵权、违规,可直接反馈本站,我们将会作修改或删除处理。
图文推荐
2021-01-31 18:49:36

2021-01-31 16:49:16
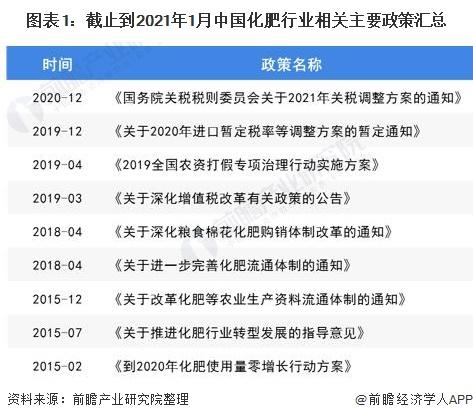
2021-01-31 15:49:13
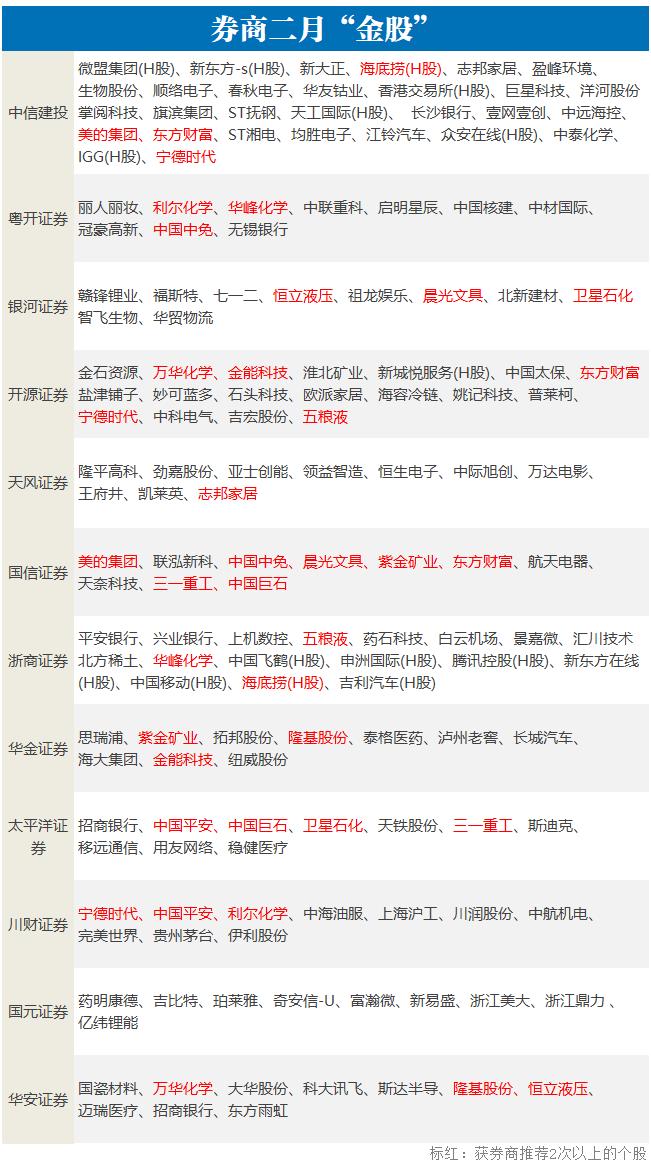
2021-01-31 13:49:05
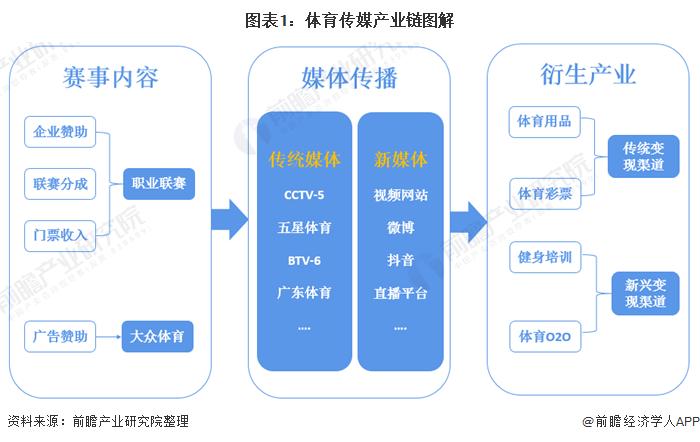
2021-01-31 10:49:04
2021-01-31 09:49:05
热点排行
精彩文章

2021-02-01 08:50:08
2021-01-31 15:49:30
2021-01-31 11:49:30
2021-01-31 07:50:07
2021-01-30 18:49:21

2021-01-30 17:51:13
热门推荐
